立项流程
发布时间:2025-03-16 作者:东莞广济医院
立项流程
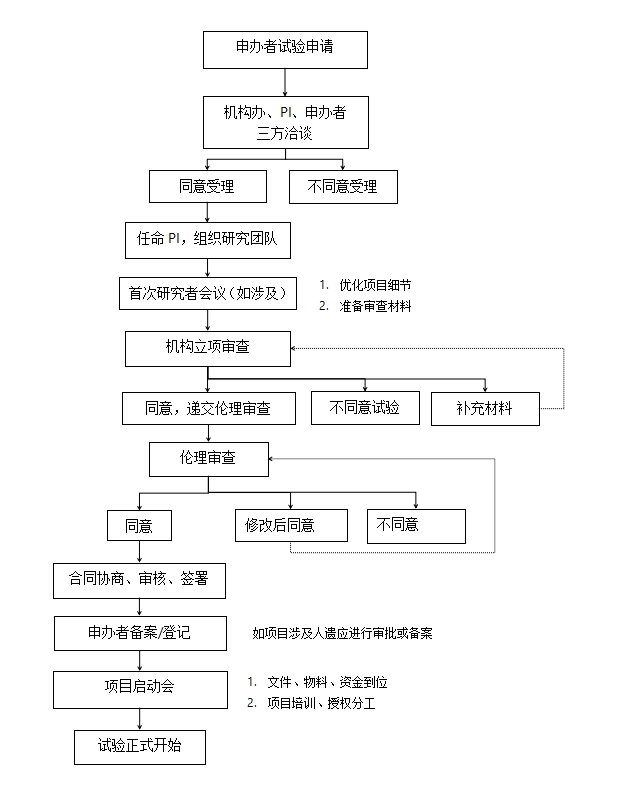
详细流程:
1.本机构药物/医疗器械临床试验项目由临床试验机构办公室统一承接。
2.申办者填写《药物临床试验申请表》/《医疗器械临床试验申请表》,提交试验申请(所有表格在“下载专区”查看)。
3.机构办公室根据受试产品的类别和技术要求与申办者共同商定负责该研究的专业组和主要研究者(以下简称PI),商定面谈时间,由申办者与PI沟通试验具体内容,专业组及PI根据科室的实际情况决定是否参与。
4.组建研究团队,如作为组长单位,PI协调组织首次研究者会议,如作为参与单位,PI及研究人员应根据项目需要参加首次研究者会议(如涉及)。
5.PI负责将《药物临床试验项目立项评估表》/《医疗器械临床试验项目立项评估表》与评估表所附《临床试验报送资料列表》要求的相应文件交专业负责人审核,审核完毕后递交机构办公室,机构进行立项审核,审核要点:科学性、合规性和可行性。
6.机构立项,PI将项目提交伦理委员会审查。
7.伦理审查通过,申办者与医院签订临床试验合同。合同参照机构合同管理制度制订,由申办者提供。
8.药物临床试验开始前,申办者应当在药物临床试验登记与信息公示平台进行药物临床试验信息登记。/医疗器械临床试验开始前,申办者向其所在地省、自治区、直辖市药品监督管理部门进行临床试验项目备案。项目如涉及人类遗传资源管理,须按规完成相应的人类遗传资源审批/备案。
9.PI需在国家医学研究信息系统进行登记。
10.项目启动前,由申办者和研究团队/机构共同商议,根据研究领域和试验方案的特点,对项目源文件(含源数据)在临床试验中的重要程度进行判定,对于以纸质方式记录的核心受控文件,如不具有唯一性和不可替换性,则应由申办者向机构办公室递交《临床试验核心文件受控盖章申请表》进行受控管理,需要盖章的文件/表格如涉及由申办者提供的,也当一并递交机构办公室。
备注:临床试验的原始记录应为受控文件。本院受控的项目文件按照: “核心受控文件”、“一般受控文件”两个受控等级,采取相应受控管理措施。纸质文件如按照一般受控文件管理,应有文件版本号、交接记录。确保文件版本的准确和防止无效版本的使用,保证文件的规范使用和数据的可靠性。如果纸质文件记录的内容与试验用药品/医疗器械的安全性评估、有效性评估数据关系密切,须确保文件的唯一性和不可替换性,则须按照“核心受控文件”进行严格的受控管理。例如:各类评分量表、受试者日记卡、试验用药品/医疗器械使用相关记录表、生物样本处理表等。
11.试验经费到账,提交《药物临床试验启动会召开申请表》/《医疗器械临床试验启动会召开申请表》,召开临床试验启动会,进行研究人员培训与授权分工。试验用药品由申办者与机构GCP药房交接,试验医疗器械由机构办公室、专业组与申办者三方共同交接,完成试验物资的交接手续,试验即可正式开展。