伦理审查申请流程
发布时间:2025-03-05 作者:东莞广济医院
伦理审查申请流程
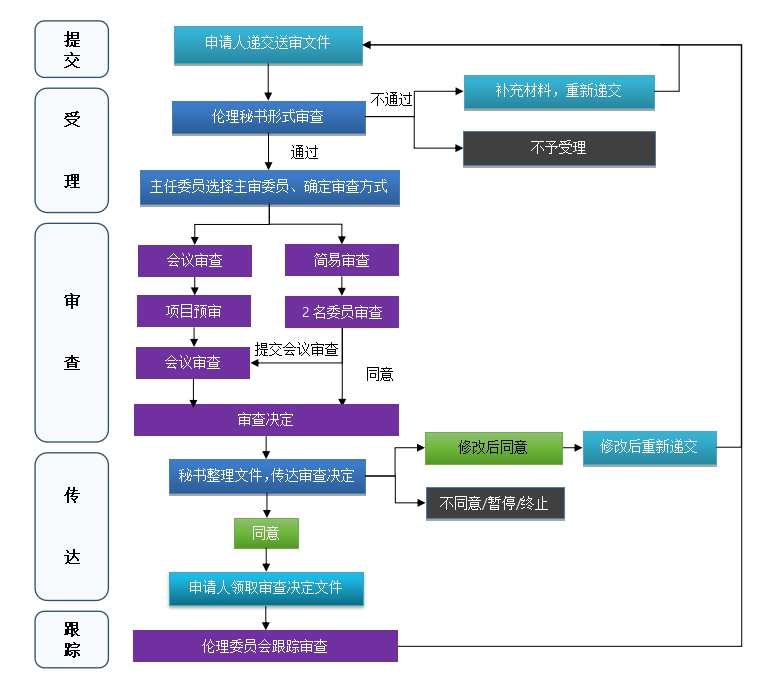
一、详细流程:
(一)申请人根据《伦理审查申请类别》,填写相应的申请表格。按照《送审文件清单》准备送审文件,以下所有表格见【附件表格】专栏。初始审查申请应同时递交《研究经济利益声明(研究者)》(F-LL-01-GLZD-2-3-0)。
(二)初始审查申请应先提交1份已签字、盖章的纸质送审文件(超过两页以上的文档双面打印),同时将电子版送审文件(PDF格式)发送至伦理委员会邮箱。送审文件通过形式审查后,须另外准备书面送审文件(复印件)12份,送至伦理委员会办公室。
(三)跟踪审查申请须提交2份已签字、盖章的纸质送审文件送至伦理委员会办公室。如审查形式为会议审查,须另外准备11份书面送审文件(复印件),送至伦理委员会办公室。
(四)形式审查如果发现送审文件不完整,文件要素有缺陷,秘书将发送《补充/修改送审材料通知》,告知缺项文件、缺陷的要素以及最近审查日期及地点。如果送审文件的完整性和要素通过形式审查,秘书将发送《受理通知》并告知预定审查日期。
(五)秘书通过电话/短信/邮件等方式通知申请人伦理审查会议时间及地点;PI参照《研究者汇报项目提纲》(F-LL-01-GZZN-1-10-X)准备汇报PPT,提前递交伦理委员会办公室,并到会汇报。
(六)召开伦理审查会议,PI应提前15分钟到达会场,申办者/CRO派出1~2名专业人员到场,必要时对委员提出的产品相关问题进行解答。
二、注意事项:
(一)免除知情同意
根据国家卫健委医学伦理专家委员会办公室、中国医院协会发布的《涉及人的临床研究伦理审查委员会建设指南》的要求:在满足下列必要充分条件时,伦理审查委员会可以同意豁免知情同意:
1.受试者可能遭受的风险不超过最低限度。
2.豁免征得受试者的知情同意并不会对受试者的权益产生负面影响。
3.利用可识别身份信息的人体材料或者数据进行研究,已无法找到受试者,且研究项目不涉及个人隐私和商业利益。
4.生物样本捐献者已经签署了知情同意书,同意所捐献样本及相关信息可用于所有医学研究。
需注意:豁免征得知情同意,不意味着免除伦理审查委员会的审查。
如需申请豁免知情同意,请同时填写并递交《免除知情同意申请》(F-LL-01-GZZN-1-11-X)。
(二)免除知情同意签字
以下两种情况可以申请免除知情同意签字:
1.研究对受试者的风险不大于最小风险,并且如果脱离“研究”背景,相同情况下的行为或程序不要求签署书面知情同意。例如,访谈研究,邮件/电话调查。
2.当一份签了字的知情同意文件会对受试者的隐私构成不正当的威胁,研究中确定受试者真实身份的唯一记录是知情同意文件,并且主要风险就来自于受试者身份或个人隐私的泄露。在这种情况下,应该遵循每一位受试者本人的意愿是否签署书面知情同意文件。
对于同意免除签署书面知情同意文件的研究项目,伦理委员会可以要求研究者向受试者提供书面告知信息。
如需申请豁免知情同意签字,请同时填写并递交《免除知情同意签字申请》(F-LL-01-GZZN-1-12-X)。
三、审查费用:
会议审查,初始审查费用:4000元/项。
简易审查,初始审查费用:2000元/项。如简易审查转为会议审查,需在伦理审查决定书送达后补交2000元/项。
修正案审查:2000元/项。
经临床试验伦理委员会审查同意的临床试验项目,在开展过程中的不依从/违背方案审查、安全性信息审查、年度/定期跟踪审查、暂停/终止研究审查、结题审查、再审不再收费。
四、审查时限:
(一)项目正式受理后,至少30天内召开会议并出具审查意见。按照递交材料先后顺序安排伦理审查会议。
(二)研究过程中出现重大或严重问题,危及受试者安全时,或发生其它需要伦理委员会召开会议进行紧急审查和决定的情况,伦理委员会将召开紧急会议进行审查,紧急会议及时召开。
(三)伦理审查决定后10个工作日内以“伦理审查批件”或“伦理审查意见”的书面方式传达审查决定。紧急会议审查决定于审查决定后及时传达,最长不超过3个工作日。如果申请人要求提前传达“同意”的决定,应尽快传达。